Застосування місцевих засобів терапії в лікуванні гострокінцевих кондилом
Г.М. Бондаренко, Ю.В. Щербакова
Інфекції, що викликані вірусом папіломи людини (ВПЛ) відносяться до найбільш розповсюджених в світі інфекційних захворювань. При цьому вони не обмежуються поширенням лише серед осіб, що належать до уразливих груп населення щодо зараження інфекціями, що передаються статевим шляхом (ІПСШ), та ВІЛ (які часто змінюють статевих партнерів, вживають наркотичні речовини, тощо), а охоплюють всі шари суспільства.
Метою даної роботи був аналіз сучасних літературних даних з питань лікування захворювань, які викликані вірусом папіломи людини, вивчення практичного досвіду і клінічного значення застосування різноманітних методів терапії.
За даними спостережень, розповсюдженість ВПЛ-інфекції серед населення варіює від 4 до 35% та безпосередньо залежить від кількості статевих партнерів.
Досліджено, що 20 % різних форм раку в жінок й 10 % у чоловіків виникають у зв’язку з попереднім зараженням папіломавірусом.
Результатом активного перебігу папіломавірусної інфекції (ПВІ) є епітеліальні новоутворення як шкіри, так і слизових, що проявляються часом через місяці, а то й роки після первинного інфікування. Традиційними органами-мішенями для ВПЛ є насамперед шкірні покриви й слизові оболонки аногенітальної ділянки та верхніх дихальних шляхів, рідше порожнини рота, стравоходу, прямої кишки, кон’юнктиви ока.
Бородавки, які є доброякісною гіперплазією шкіри, зустрічаються найчастіше. За даними американських дослідників, вони становлять близько 8% діагнозу усіх пацієнтів дерматологічного прийому.
У загальній популяції бородавки виявляються в 7-10%, переважно в дітей шкільного віку й молодих людей. ВПЛ стійкі до холоду й високих температур і передаються безпосередньо в процесі контакту. Передачі інфекції сприяють мікротравми, відвідування басейнів і спортивних залів.
У дітей ПВІ найчастіше представлена простими бородавками. Захворюваність у дитячому віці, за різними даними, становить від 3 до 20%. Вважають, що ПВІ в дітей носить транзиторний характер, і активні прояви вірусу зникають у результаті ефективної імунної відповіді. Зараження може відбуватися як від матері-носійки ПВІ (внутрішньоутробно, трансплацентарно або в процесі пологів), так і пізніше в процесі життя.
За деякими даними, представники таких професій як м’ясники, ветеринари, працівники рибопереробних виробництв мають підвищений ризик захворюваності на бородавки в ділянках кистей рук, обумовлені ВПЛ 7-го типу.
За даними дослідників, у пацієнтів з проявами плоскоклітинного раку шкіри, а також з преепітеліоматозами (актинічний кератоз) спостерігається підвищений вміст у сироватці крові антитіл до ДНК ВПЛ.
За деякими даними, ВПЛ 1-го і 2-го типів, асоційовані з carcinoma in situ (хвороба Боуена).
Зв’язок ПВІ з неоплазіями епідермального походження підтверджується існуванням такої нозологічної форми, як бородавчаста епідермодисплазія, рідкісним генодерматозом, з притаманною йому імуногенетичною схильністю до інфекції шкіри, обумовленою ВПЛ 5-го і 8-го типів. Це – хронічні дисеміновані висипання ПВІ і, оскільки дані типи ВПЛ є онкогенними, в цих пацієнтів уже у віці 30-40 років можуть спостерігатися множинні висипання, характерні для плоскоклітинного раку шкіри, на відкритих ділянках шкіри.
Гострокінцеві кондиломи в деяких літературних джерелах називаються «генітальними бородавками», термін, що підкреслює етіологію цих утворень. ПВІ слизової та перехідної частини епітелію є найпоширенішою ІПСШ, і зустрічається вдвічі частіше, ніж генітальний герпес. ПВІ геніталій має тенденцію до постійного зростання і становить на сьогодні серйозну проблему для здоров’я населення, особливо з огляду на онкогенну роль окремих типів ВПЛ слизових (16 і 18) у розвитку раку шийки матки й, можливо, карциноми слизової анального отвору.
В аногенітальній ділянці зазвичай виявляють ВПЛ типів 6, 11, 16, 18,31, 33, 35, 41 й 42, причому можлива наявність в одного хворого декількох типів вірусу одночасно. Онкогенні можливості притаманні також ВПЛ-31, 33, 35, 38-40, 51-55. Аногенітальні бородавки (гострокінцеві кондиломи) є лише частиною спектра уражень, викликаних ВПЛ.
Клінічні прояви ПВІ у вигляді кондилом спостерігаються в 3-5% людської популяції, в 10-15% населення має місце прихований перебіг інфекції, що розцінюється як «резервуар» і джерело інфекції у разі її реактивації. За іншими даними, асимптомне носійство ВПЛ має місце в 25% жінок у віці до 25 років.
За даними спостережень, гострокінцеві кондиломи зустрічаються приблизно у 1% сексуально-активного населення США, на їх частку також доводиться 25% всіх діагнозів, встановлених в клініках сечостатевої медицини Великої Британії. За даними епідеміологічних досліджень, середній вік тих, хто хворіє на кондиломи, в Європі становить 31 рік, віковий «розкид» складає від 2 до 68 років з піком захворюваності у віці 20-24 роки.
В аналізі факторів ризику інфікування ВПЛ і розвитку неопластичних процесів особлива увага приділяється ранньому початку статевого життя (дія канцерогенних факторів на незрілий епітелій шийки матки), частій зміні статевих партнерів, наявності супутньої урогенітальної інфекції, використанню оральних контрацептивів, тощо. Більшість випадків кондилом аногенітальної локалізації є результатом статевого контакту. За статистикою, більше половини жінок — статевих партнерок чоловіків, котрі мають кондиломи, також заражені ВПЛ. Число заражених серед чоловіків – статевих партнерів жінок, які страждають на кондиломи, ще вище (від 49 до 94% за різними даними). Перианальна локалізація кондилом цілком може бути результатом нестатевого зараження, однак високе розташування кондилом по ходу прямої кишки, на думку багатьох авторів, носить, безперечно, статевий характер. В 65-70 % випадків гострокінцеві кондиломи виявляють при обстеженні обох статевих партнерів. Передача ВПЛ сексуальному партнерові в одностатевих парах в 5-10 разів частіше, ніж у гетеросексуалів. Доведено, що онкогенний фрагмент геному ВПЛ присутній на сперматозоїдах.
Можна виділити наступні форми перебігу ПВІ статевих органів:
1) латентна (відсутність клінічних проявів і морфологічних ознак при визначенні ДНК ВПЛ);
2) субклінічна (мінімально виражена клініка, мінімальні морфологічні ознаки альтерації при визначенні ДНК ВПЛ);
3) клінічна (активні клінічні прояви у вигляді кондилом і дисплазії різного ступеня виразності при визначенні ДНК ВПЛ).
Слід пам’ятати, що існує висока вірогідність зараження ПВІ дітей, з подальшою появою в них гостокінцевих кондилом. Можливі три шляхи передачі інфекції: перинатальний (внутрішньоутробно, у процесі пологів), горизонтальний (самозараження й «нестатеве» зараження при контакті), зараження внаслідок сексуального насильства.
Науковцями продемонстровано існування кондиломатозу гортані й анальних кондилом у немовлят від матерів з активними клінічними проявами кондилом. Відомі випадки самозараження перианальної ділянки внаслідок перенесення вірусу від звичайних бородавок на кистях. У такий же спосіб може відбуватися гетерозараження як прямого, так і непрямого інфікування внаслідок користування спільними ваннами й рушником. Описано випадки ятрогенної передачі ПВІ, через нестерильні інструменти, медичні рукавички, вапоризовану інфіковану тканину після лазерної деструкції.
За даними спостережень встановлено, що у віці дитини до 3-х років має місце перинатальне зараження, підтвердженням чому служить виявлення вцих випадках здебільшого ВПЛ 2-го типу (тобто вірус звичайних бородавок). У віці дитини старше 3-х років і в разі виявлення в утвореннях ВПЛ-6 або -11 типів, можна припускати статевий шлях зараження, тоді як наявність у цьому віці ВПЛ-2 типу свідчить про самозараження або інше походження, відкидаючи статевий шлях.
У чоловіків кондиломи локалізуються здебільшого в ділянці крайньої плоті, по вінцевій борозні, на голівці статевого члена. За даними літератури, в 20-25% випадків може спостерігатися також внутрішньоуретральна локалізація кондилом, здебільшого на межі 1,5 см від виходу уретри (човнувата ямка). Перианальна локалізація можлива в гетеросексуалів, але частіше зустрічається в гомосексуалістів. Можлива також інша локалізація – мошонка, пахові складки.
У жінок висипи, як правило, локалізуються навколо входу в піхву, на малих та великих статевих губах. Внутрішньоуретральна локалізація зустрічається набагато рідше, ніж у чоловіків (4-8% випадків). У 20% випадків має місце перианальна локалізація.
Локалізація висипань усередині заднього проходу, особливо множинні висипання, зустрічаються здебільшого в осіб з неодноразовими анальними статевими контактами або в разі імуносупресії.
Негенітальна локалізація кондилом, а саме в ділянці червоної облямівки губ, гортані, на слизовій ротової порожнини спостерігається рідко й найчастіше пов’язана з імуносупресією.
Інкубаційний період при зараженні ПВІ варіює від 3 тижнів до 9 місяців (у середньому — 3 місяці). Вірус, потрапляючи на шкіру або слизову оболонку, проникає в клітину й впроваджується в ядро. Він може залишатися там у неактивному стані довгий час. За певних умов зниження захисних сил організму вірус починає розмножуватися в ядрі, викликаючи проліферацію епітеліальної тканини, й проникає в інші клітини.
У наукових дослідженнях для визначення білків вірусної оболонки всіх типів ВПЛ застосовуються імунологічні методи з використанням пероксидазної й антипероксидазної реакцій. Для ідентифікації типу вірусу використовуються методи молекулярної біології, у тому числі ДНК-гібридизації та полімеразно-ланцюгової реакції (ПЛР). Точне визначення фізичного статусу ДНК ВПЛ у клітині надзвичайно важливе для прогнозування розвитку неопластичних процесів.
Особливістю циклу інфікування ВПЛ є можливість уникати імунної відповіді. В глибоких прошарках базального шару епітелію, де персистує ВПЛ, реплікація вірусу мінімальна, клітинний лізис відсутній, тому розпізнавання вірусу імунною системою незначне. По мірі наближення до рогового шару епітелію, зі зростанням ступені диференціації клітин епітелію, прискорюється реплікація вірусної ДНК. У процесі десквамації епітелію проходить відшарування навантажених вірусом епітеліальних клітин та таким чином «уникання» імунної відповіді організму.
Незважаючи на велику кількість рекомендацій з лікування ПВІ, вони здебільшого носять загальний характер, і не завжди можуть застосовуватися в повсякденній практиці.
Сучасні рекомендації по лікуванню генітальних бородавок, включають в себе як самостійну терапію, так і лікування, яке проводить лікар.
Жоден із пропонованих на сьогоднішній день методів лікування не забезпечує відсутність рецидивів, наявність яких можна трактувати як неуспіх в лікуванні.
Багато авторів звертають увагу на можливий спонтанний регрес висипань, що може спостерігатися не тільки при бородавках, але також при кондиломатозі, включаючи дисплазію III ступеня. За деякими даними, спонтанний регрес кондилом простежувався в 20-30% випадків свіжого зараження, тобто протягом перших 6 місяців існування активних проявів. Але він виключений у пацієнтів у стані імуносупресії.
Специфічного лікування бородавок і кондилом на цей час не існує. Мета лікування: зникнення макроскопічно видимих уражень шкіри, що досягається різними деструктивними методами, а саме хімічною деструкцією й різними аблятивними методиками.
За даними закордонних авторів, лікування бородавок і кондилом потребує значних витрат, оскільки як мінімум 20% всіх пацієнтів для досягнення бажаного результату від лікування змушені відвідувати лікаря понад 10 разів.
Методи, які застосовуються в лікуванні уражень шкіри та слизових оболонок, що викликані ВПЛ можна розподілити на декілька груп:
- Хімічна деструкція (солкодерм, ферезол, трихлороцтова кислота 80-90%);
- Фізична деструкція (хірургічне висічення, кріодеструкція, лазерна деструкція, електрокоагуляція тощо);
- Антимітотичні препарати (подофілін 10-25%, подофілотоксин 0,5%, епіген-спрей, 5-фторурациловий крем 5%).
- Імунотерапія із застосуванням інтерферонів і їх індукторів (циклоферон, інтерферон, тощо).
- Топічні модифікатори імунної відповіді («Алдара»- іміквімод 5% крем,
Установлено, що після деструкції видимих висипань вірус персистує у зовні здоровому епідермісі, призводячи до частих рецидивів (близько 30%). За різними даними, ефективність лікування екзофітних кондилом становить від 50 до 94%. При цьому найбільш поширеними є аблятивні техніки, які також визнаються найефективнішими, тобто забезпечують зникнення висипань після одноразової обробки.
При хірургічному висіченні, кріодеструкції, лазерній деструкції та електрокоагуляції відсоток повного зникнення висипань становить від 31 до 93%. Однак ці ж способи лікування дають високий відсоток рецидивів у перші 3 місяці після лікування (від 21 до 95%). Приблизно такі ж результати було отримано при абляції новоутворень за допомогою інфрачервоного коагулятора, з тією лише різницею, що ступінь запальної післяопераційної реакції була набагато меншою, і відповідно строки загоєння були коротшими.
За даними аналізу літератури, проведеного комітетами доказової медицини (Cochrane Central Register of Controlled Trials), щодо ефективності зовнішньої терапії шкірних бородавок в імунокомпетентних пацієнтів лише застосування саліцилової кислоти й кріотерапії не викликає сумнівів з погляду методології і статистичної репрезентативності. При цьому як кератолітики, так і кріотерапія, на думку широкого загалу фахівців, є методами лікування «першої лінії», у той час як, наприклад, вапоризацію новоутворень вуглекислотним лазером рекомендують застосовувати у випадку резистентного, персистуючого й рецидивуючого перебігу ПВІ. З іншого боку, для лікування кондилом кріотерапія не є цілком вдалим методом лікування, оскільки метод болісний, дає високий відсоток рецидивів.
За даними літератури, застосування цитостатичних препаратів, імунотерапії та хімічної деструкції не забезпечує моментального зникнення екзофітних висипань, однак забезпечує зниження рівня рецидивів (11-36%).
Застосування антимітотичних препаратів обумовлено прагненням мінімізувати побічні ефекти загального лікування, між тим вони не виключають місцевого токсичного впливу. До цієї групи належать подофілін і подофілотоксин, 5-фторурацил, сульфат блеоміцину й ін. За даними літератури, ці препарати не мають переваг перед іншими методами. У процесі лікування завжди відзначається більш-менш виражена запальна реакція на місцеве нанесення препарату, що, очевидно, також є елементом лікування, поряд з прямою антимітотичною і цитостатичною дією, активізувати механізми місцевої імунної відповіді.
Подофілотоксін протипоказаний при вагітності. Тому слід рекомендувати жінкам дітородного віку застосовувати методи контрацепції або утримуватися від сексуальних контактів під час терапії.
Незважаючи на певний арсенал препаратів і методик для лікування новоутворень ПВІ, жоден з них не є етіотропним і патогенетично обґрунтованим і не забезпечує остаточного припинення процесу появи нових висипань та їх поширення.
Показано ефективність інтерферонів при утвореннях ПВІ, а також у разі вірусних ускладнень при трансплантації органів на тлі застосування імунодепресантів, однак вона менш вивчена. Переважна більшість клінічних спостережень пов’язана із застосуванням рекомбінантних альфа-інтерферонів різних фірм (реаферон, реальдерон, роферон А, інтрон А, берофор і ін.).
Різноманітність клінічних ефектів інтерферонів пов’язана з трьома відомими механізмами їхньої дії – антивірусною, імуномодулюючою, антитуморогенною. Разом з тим, широке використання інтерферонів дало змогу виявити низку таких небажаних побічних ефектів, як: грипоподібний синдром, цукровий діабет, захворювання щитоподібної залози, синдром депресії, автоімунний синдром тощо.
Як правило, зазначені негативні явища спостерігаються внаслідок передозувань або тривалих, багатомісячних курсів лікування інтерфероном, що не є випадком лікування активних проявів ПВІ. Варто зауважити, що частота виявлення перерахованих ускладнень не перевищує 1,5 %, причому більшість із них мають оборотний характер і зникають після відмінення препаратів.
Незважаючи на успіхи імунотерапії, ефективність лікування кондилом у хворих на ВІЛ не перевищує таку при традиційних методах лікування, напевне, причина в тому, що мобілізація місцевого імунітету в цьому випадку є проблематичною.
За даними дослідників, до клінічно найбільш перспективних низькомолекулярних індукторів належать циклоферон, аміксин, а також деякі високомолекулярні природні й синтетичні полімери – лорифан, полудан, кагоцел. Попри те, що активність індукторів практично аналогічна активності інтерферонів, індуктори мають свої точки дотику в імунній системі. Наприклад, аміксин викликає повільну продукцію інтерферону Т-лімфоцитами, а циклоферон викликає термінову продукцію інтерферону В-лімфоцитами.
Досягти підвищення ефективності лікування шкірних форм ПВІ можна також за рахунок комбінації декількох методів, у тому числі імунотерапії з деструкцією.
В лікуванні епітеліальних новоутворень, викликаних ПВІ, також застосовувалися топічні ретиноїди, топічний вітамін D3, гелі диклофенаку на основі гіалуронової кислоти, що використовуються для зовнішнього лікування новоутворень епітеліального походження іншого генезу (себорейні, актинічні кератоми, інші преканкрози). Однак механізм їхньої дії остаточно не вивчений, а тому ефективність препаратів, за різними джерелами, відрізняється.
Принципово новим направленням в лікуванні активних проявів ПВІ є застосування вакцини проти ВПЛ високого онкогенного ризику (16, 18), спрямоване на профілактику рака шийки матки. Даний вид лікування відрізняється специфічністю дії, однак належить уточнити показання до застосування вакцини, категорії пацієнтів, належних до вакцинації.
За даними закордонних авторів, лікування бородавок і кондилом потребує значних витрат, оскільки як мінімум 20% всіх пацієнтів для досягнення бажаного результату від лікування змушені відвідувати лікаря понад 10 разів. Що не є зручним як для пацієнта, так і для лікаря. Більшість методів терапії ПВІ потребує додаткового обстеження та/або проведення лікування лікарем.
В лікуванні уражень шкіри та слизових, що викликані ВПЛ, з успіхом використовується хіміотерапевтичний засіб для місцевого застосування Алдара, 5% крем іміквімоду. Цей метод терапії відноситься до методів так званої «першої лінії», коли топічне лікування може проводитись пацієнтом під контролем лікаря.
Іміквімод – модифікатор імунної відповіді. Засобу не притаманна пряма антивірусна активність. Іміквімод стимулює як вроджений так і набутий імунітет. На реакції вродженого імунітету вплив відбувається шляхом активації Toll-подібних рецепторів, що експресовані моноцитами, макрофагами і дендритними клітинами, яка індукує продукцію цитокінів та хемокінів, залучених до реакції вродженого імунітету. Продукуються цитокіни: IFN-a, TNF-a, інтерлейкіни (IL-1, -5, -6, -8, -10, -12) та хемокіни: GM-CSF, MIP-1a, MIP-1b, MCP-1. Також відбувається стимуляція активності природних кілерів (NK-клітин).
Також іміквімод спричиняє вплив на клітинний імунітет. Підсилює міграцію клітин Лангерганса в регіонарні лімфатичні вузли, що посилює презентацію антигенів T-клітинам. Цитокіни (такі як IL-12 і TNF) стимулюють секрецію IFN-g NK-клітинами та T-лімфоцитами. При гістологічному дослідженні біоптатів шкіри при лікуванні іміквімодом спостерігається лімфоцитарна інфільтрація.
Завдяки стимуляції вродженого імунітету отримується швидка, неспецифічна загасаюча відповідь, яка приводить до регресії симптомів. А завдяки впливу на адаптивний клітинний імунітет спостерігається повільна, специфічна відповідь, що приводить до ремісії.
Також іміквімод індукує апоптоз ракових клітин шкіри. Результати досліджень invivo&invitro вказують на те, що іміквімод викликає апоптоз клітин пухлин. Це відбувається в обхід механізмів стійкості до апоптозу, притаманних пухлинним клітинам. Іміквімод стимулює викид цитохрому С в мітохондріях Bcl-2-залежним шляхом і індукує каспазу-3. Ефект іміквімоду не залежить від активації рецептора CD95 (системи рецепторів FAS / APO-1) або системи рецепторів TRAIL. Прямий і селективний ефект індукції апоптозу клітин пухлин дає ефект синергізму з його імуномодулюючими властивостями, що прискорює видалення епітеліальних пухлин.
З самого початку імунотерапія іміквімодом позиціонувалася як лікування новоутворень ВПЛ на слизових оболонках. До переваг даного методу лікування також належить стійкість терапевтичного результату, що, очевидно, можна пов’язати з корекцією місцевого імунітету в процесі лікування.
Проводилося рандомізоване, подвійне сліпе, плацебо контрольоване порівняльне дослідження (L. Edwards, A. Ferenczyetal.) для оцінки ерадикації бородавок у 311 пацієнтів віком від 18 років, з кількістю зовнішніх аногенітальних бородавок від 2 до 50. Результати лікування іміквімодом, згідно з отриманими даними, по закінченні лікування дали 13% рецидивів протягом перших трьох місяців й забезпечили безрецидивний стан у наступні 3 місяці, що значно нижче відсотка рецидивів при загальноприйнятих методах лікування.
За результатами рандомізованого, порівняльного дослідження (H. Schofer, A. Van Ophovenetal) довгострокової ефективності 5% крему іміквімод і звичайних методів абляційних терапії при лікуванні зовнішніх аногенітальних бородавок, іміквімод крем 5% в якості монотерапії (93,7%) або в комбінації з абляцією (91,5%) виявився ефективнішим, ніж тільки абляційна терапія (73,6%), що проявилося в вірогідній відміні — зменшенні частоти рецидивів успішно вилікуваних бородавок аногенітальної області
Отримані дані клінічного дослідження, де з’ясовували ставлення пацієнтів до наявності у них генітальних бородавок і до лікування цих бородавок препаратом іміквімод та іншими методами. Було встановлено, що пацієнти оцінили 5% крем іміквімод як ефективний засіб лікування, який призводить до зникнення бородавок за прийнятний період часу (у 78% пацієнтів це відбулося вже протягом перших 4 тижнів), викликає мінімальну болісність і зручний в застосуванні.
В дослідженні, що проводилося в різних центрах Європи, Канади, Мексики, Латинської Америки, Австралії та Південної Африки (O’Mahonyetal), спостерігали пацієнтів відносно часу зникнення геніальних бородавок, зручності застосування та відсутності болю при проведенні лікування та задоволення результатами терапії. Більше 60% пацієнтів оцінили іміквімод вище, ніж подофілін та трихлороцтову кислоту та більше 50% пацієнтів — вище, ніж кріо- та лазерну терапію.
При виникненні місцевих реакцій в області нанесення препарату при застосуванні іміквімоду при необхідності можна зробити паузу в кілька днів. В пілотних клінічних дослідженнях(G. Von Kroghetal) зникнення бородавок спостерігалося у 56% пацієнтів. Більший відсоток жінок (77%) порівняно з чоловіками (40%) відзначили зникнення бородавок. У дослідження увійшли, здебільшого, чоловіки після циркумцизії. Медіана часу до зникнення бородавок у жінок виявилася менше (8 тижнів) порівняно з чоловіками (12 тижнів). Був відзначений низький відсоток рецидивів (13%).
Іміквімод-крем (препарат «Алдара»), що випускається в пакетиках для одноразового застосування, наноситься на бородавки 3 рази на тиждень перед сном, а на наступний ранок ділянку нанесення очищується водою і м’яким милом. Лікування триває до зникнення бородавок, але не більше 16 тижнів.
Шкірні реакції на іміквімод зазвичай розвиваються після 3-4 тижнів (для порівняння, на подофіллотоксін- на 3 день терапії). Більшість з них проходить самостійно під час паузи між застосуваннями в кілька днів. Рідкісним ускладненням є болісні ерозії або набряк при терапії множинних кондилом в препуциальному мішку статевого члена. Пацієнтам слід порадити звернутися до лікаря при виникненні даного ускладнення. Симптоматична терапія включає в себе місцеве застосування кортикостероїдів до поліпшення стану.
Таким чином, останнім часом відзначається зростання кількості звернень в клініки з лікування ІПСШ. Доцільним представляється використання методів лікування, здатних привести до зниження кількості візитів до лікаря. Рішенням проблеми є застосування препаратів для терапії в домашніх умовах. Окрім того, особливої уваги заслуговують методи лікування з низьким рівнем рецидивів.
Цим вимогам відповідає засіб іміквімод. Наведені дані свідчать про те, що терапією вибору при лікуванні гострокінцевих кондилом є іміквімод (Альдара). Він показаний до застосування як для чоловіків, так і для жінок.
Іміквімоду притаманні: висока ефективність, здатність знизити кількість рецидивів. Препарат рекомендований до застосування в лікуванні гострокінцевих кондилом міжнародними керівництвами (Європейське керівництво з лікування ІПСШ (IUSTI); American Medical Association Consensus Conference (консенсус американської медичної асоціації), ECHPV (Європейський Курс з HPV- асоційованої патології); Sexually Transmitted Diseases Treatment Guidelines, CDC (Керівництво з лікування ЗПСШ Центра з контролю та попередження захворювань).
Засобу іміквімод віддають перевагу більшість пацієнтів, що підтверджено спостереженнями.
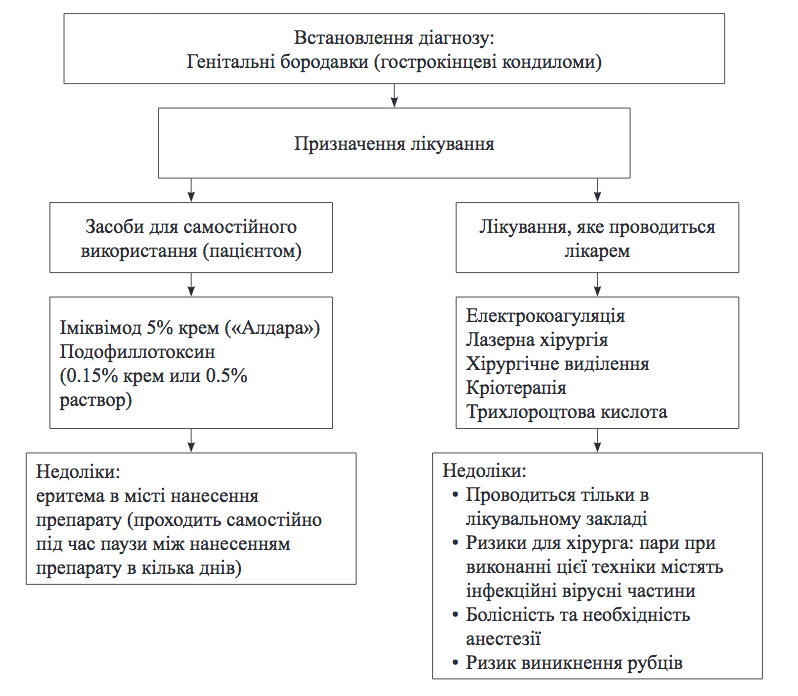
Алгоритм вибору терапії гострокінцевих кондилом представлений на рис. 1.